Saúde do osso e câncer de mama
O tratamento do câncer de mama muitas vezes causa a redução dos hormônios femininos circulantes, levando a uma maior fragilidade dos ossos. Desta forma, cuidar da saúde óssea é muito importante, para evitar a osteopenia e, posteriormente, a osteoporose.
A osteoporose é uma doença em que a resistência óssea é comprometida, aumentando a fragilidade dos ossos e a suscetibilidade a fraturas por traumas mínimos ou por queda da própria altura. A perda da resistência óssea normalmente ocorre de forma silenciosa e progressiva, sem sintomas, até a primeira fratura ocorrer. O risco de novas fraturas dobra pela ocorrência de uma fratura prévia, independentemente de qualquer outro fator de risco associado.
As fraturas causadas pela osteoporose (punho, quadril e coluna) podem ter uma importante repercussão na saúde dos pacientes, resultando em dor crônica, perda da mobilidade, dependência permanente e morte por complicações do tratamento.
Como ocorre a osteoporose em pacientes com câncer de mama?
O câncer de mama e a osteoporose são diagnósticos comuns em mulheres e estão frequentemente interligados (idade e estado hormonal). O risco de câncer de mama aumenta com a idade, sendo elevado em pacientes com idade superior a 60 anos, assim como o risco de osteoporose.
A terapia de supressão hormonal (ou hormonioterapia) está indicada em mulheres pré e pós-menopáusicas com câncer de mama com receptores hormonais presentes (RE/RP). Esta supressão hormonal tem como consequência a privação de estrogênio nestas mulheres, o que acelera o turnover ósseo e pode levar a uma diminuição da densidade mineral óssea (DMO) e a um aumento de 40% a 50% na incidência de fraturas.
A resistência óssea das pacientes com diagnóstico de câncer de mama pode ser comprometida pelas condições clínicas do paciente (idade, estado hormonal), pelo tratamento adjuvante (quimioterapia, radioterapia, ooforectomia ou terapia endócrina) e pela evolução da própria neoplasia.
Os análogos do GnRh (ou LHRH) são utilizados para induzir supressão ovariana reversível em mulheres pré-menopausicas. A privação estrogênica induz à perda da DMO e aumenta o risco de fraturas. A terapia endócrina com tamoxifeno, que é um modulador seletivo dos receptores de estrogênio, tem ação antagonista ao estrogênio na mama, independentemente do estado hormonal da paciente (menacme ou menopausa); já no osso, sua ação é antagonista ao estrogênio na pré-menopausa (não protege contra a perda da DMO) e agonista na menopausa (protege contra a perda da DMO).
Nas pacientes pré-menopáusicas, o uso de tamoxifeno foi associado à perda óssea na coluna, de cerca de – 4,6% após 3 anos de uso. No entanto, tal perda óssea não representa um problema clínico que exija medicação para proteção óssea. Mas o risco de fraturas aumenta significativamente quando a paciente utiliza análogos do GnRH para supressão e a seguir utiliza tamoxifeno. Neste caso, a ação do agonista do tamoxifeno no osso é insuficiente para neutralizar a rápida perda óssea associada à privação hormonal.
Nas pacientes pós-menopáusicas em uso de tamoxifeno, observou-se ganho ósseo anual de 0,5-1% na coluna e redução de 30% no risco de fraturas. O tamoxifeno reduz a incidência de fraturas em comparação com o placebo, em um ambiente ósseo de baixo estrogênio e, portanto, não contribui para a perda óssea relacionada à terapia endócrina nessa população.
Os inibidores aromatase (anastrozol, letrozol e exemestano) inibem a conversão periférica de androgênios em estrogênio pela enzima aromatase, reduzindo, assim, de forma rápida e importante, os níveis circulantes de estradiol. Esta classe de medicamentos está associada a aumento da incidência de fraturas, induzindo uma perda adicional de osso trabecular (coluna) de 1- 3% ao ano e aumentando a incidência de fraturas.
Após 5 anos de uso de tamoxifeno o uso subsequente de inibidores da aromatase determina uma redução na DMO de 5,3% em 24 meses, com uma taxa de fratura de 3%/ano. A perda óssea é ainda maior em mulheres pós-menopáusicas usando inibidores da aromatase e que não fizeram uso prévio de tamoxifeno, com perda de 6,1% da DMO da coluna em 5 anos e com aumento do risco de fraturas de 3 a 12%, após 5 anos. Ocorre ainda redução dos valores de escore trabecular (TBS). Nos casos de tratamento de inibidores da aromatase por 10 anos, o risco de fratura aumenta ainda mais.
Nos casos de pacientes pré-menopáusicas que receberam quimioterapia, aquelas que entram em amenorréia ou menopausa precoce após o tratamento quimioterápico podem perder entre 3 – 7% da DMO da coluna no 1º ano. Nas pacientes que voltam a menstruar, a DMO permanece estável e não há necessidade de controle da massa óssea. Não há evidências claras do efeito direto da quimioterapia na perda óssea em mulheres na pós-menopausa.
O mecanismo da perda óssea induzida pela radioterapia ainda não foi totalmente elucidado, mas provavelmente esteja relacionado a alterações na medula e vascularização óssea. A radioterapia está associada a um pequeno aumento (<2%) na ocorrência de fraturas nas costelas da região irradiada.
Nas pacientes pré-menopáusicas submetidas a ooforectomia (retirada dos ovários), ocorre perda significativa da DMO após 12 meses da cirurgia. Nas pós-menopáusicas não há estudo conclusivo.
Diagnóstico e manejo de pacientes em risco de perda óssea acelerada pelo tratamento do câncer de mama
– Solicitar densitometria óssea antes do início do tratamento;
– Determinar o risco individual de cada paciente para que seja encaminhada para a orientações e tratamentos preventivos caso seja necessário;
– A seleção de pacientes em risco de perda óssea acelerada pelo tratamento depende de dados da medida da densidade mineral óssea, da existência de fraturas por fragilidade, da existência de causas secundárias de perda óssea e da existência de fatores clínicos que aumentem o risco de fraturas.
Avaliação dos pacientes antes do tratamento:
1) Densitometria óssea da coluna PA e fêmur em todos os pacientes: a avaliação é sempre realizada em 2 segmentos válidos (coluna e fêmur), até 3 meses do inicio da terapia de supressão ovariana. A DMO do antebraço pode deve ser medida nas seguintes circunstâncias:
– quando quadril e/ou coluna não podem ser avaliados ou interpretados (cirurgia ou fratura prévia);
– na presença de hiperparatireoidismo;
– em pacientes muito obesas (acima do limite de peso da mesa de exame).
Obs.: na coluna lombar também avalia-se o escore trabecular como ferramenta para avaliação da microarquitetura óssea.
Todos pacientes com DMO T-Score (ver figura 1) ou Z-score < -2.0 devem realizar exames laboratoriais para exclusão de outras causas associadas à perda óssea.
2) Pesquisa de fraturas (Coluna T7 a L4) e quadril: pesquisa de fraturas vertebrais por densitometria (Vertebral fracture assessment) e raio-X de quadril e punhos.
3) Avaliação clínica e laboratorial para exclusão de causas adicionais associadas à perda óssea, além da doença de base e tratamentos associados;
– Hemograma, 25(OH)D (vitamina D), cálcio e fósforo séricos, PTH, TSH, uréia, creatinina, calciúria de 24 horas, fosfatase alcalina, albumina, proteína c reativa, enzimas hepáticas e eletroforese protéica,
4) Pesquisa de fatores que aumentam o risco de fraturas;
– Idade superior a 65 anos; terapia com inibidores aromatase > 6 meses; menopausa precoce; menopausa induzida pela quimioterapia; familiar de 1º grau com fratura de quadril; uso de tamoxifeno na pré-menopausa; fratura prévia por fragilidade após 50 anos; tabagismo; consumo de álcool (> 3 doses/dia); uso de corticosteróides; índice de massa corporal < 20; T-Score < -1,5.
Figura 1 – Curva de referência Densidade Mineral Óssea (DMO) da coluna lombar em mulheres de 10 a 85 anos demonstrando a classificação da Organização mundial de Saúde (OMS).
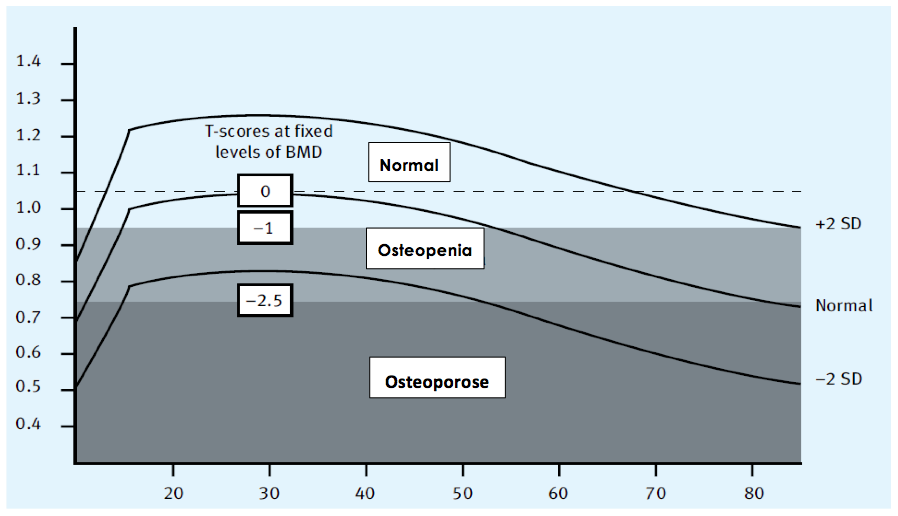
Manejo das pacientes avaliadas
Objetivo: orientação e seleção de pacientes para o estabelecimento de medidas preventivas. O gerenciamento da perda óssea associada a terapias contra o câncer inclui recomendações nutricionais, mudanças de estilo de vida e intervenção farmacológica. As pacientes consideradas de alto risco devem ser encaminhados a intervenção farmacológica com antirreabsortivos para prevenção da perda óssea associada à terapia.
1) Medidas de orientação essenciais para saúde óssea:
– Aporte proteico de 1.0-1.2g por kg peso/dia ou 20-25g proteína a cada refeição;
– Dieta rica em cálcio na pós-menopausa, com 1000 mg/dia;
– Vitamina D3 800 UI/dia ou 25 (OH)D > 20ng/ml;
– Manutenção do peso adequado com IMC >19kg/m² e <30kg/m²;
– Exercícios físicos de resistência regulares.
2) Mudança no estilo de vida:
Todas as pacientes com risco de perda óssea devem ser aconselhadas a mudanças no estilo de vida para correção de fatores que aumentam o risco de fraturas. É necessário incentivar a parada com o tabagismo assim como o consumo excessivo de álcool. Corrigir o sedentarismo e prevenir quedas também são importantes medidas.
3) identificação de pacientes em risco:
3.1) Pacientes na pré-menopausa
3.1.1) Pacientes na pré-menopausa sem uso de inibidores da aromatase:
Alto risco de fraturas se DMO T-score < -2.0 DP:
– orientações gerais sobre dieta;
– exercícios e mudanças de estio de vida;
– uso de antirreabsortivos;
– repetir densitometria em 24 meses;
Médio risco de fraturas se T-score > -2.0 e < – 1 DP:
– orientações gerais sobre dieta
– exercícios e estilo de vida
– repetir densitometria em 24 meses e, no retorno, se o T-score for < -2.0 DP ou houver perda >4% na coluna ou fêmur, encaminhar para tratamento com antirreabsortivos. Manter vitamina D > 20ng/l.
Baixo risco de fraturas se T-score > – 1.0 DP:
– orientações gerais sobre dieta, exercícios e estilo de vida.
3.1.2) Pacientes na pré-menopausa com uso de inibidores da aromatase:
Alto risco de fraturas: T-score < -1.0 DP:
– orientações gerais sobre dieta;
– exercícios e estio de vida;
– uso de antirreabsortivos;
– repetir densitometria em 24 meses.
Médio risco de fraturas T-score > -1.0:
– orientações gerais sobre dieta, exercícios e estilo de vida
– repetir densitometria em 24 meses e, se no retorno o T-score for <-2.0 DP ou houver perda >4% na coluna ou fêmur, encaminhar para tratamento com antirreabsortivos. Manter vitamina D >20ng/l.
3.2) Pacientes na pós-menopausa
3.2.1) Pacientes na pós-menopausa com uso de Inibidores da aromatase:
Alto risco de fraturas se T-score < – 2.0 DP, idade > 75 anos, 2 fatores de risco e qualquer DMO:
– orientações gerais sobre dieta;
– exercícios, modificações no estilo de vida e uso de antirreabsortivos;
– repetir densitometria em 24 meses.
Médio risco de fraturas se T-score > -2.0 e >-1.0:
– orientações gerais sobre dieta;
– repetir densitometria em 24 meses e, nos casos em que o T-score for <-2.0 DP ou houver perda >4% na coluna ou fêmur, encaminhar para tratamento com antirreabsortivos. Manter vitamina D >20ng/l.
Obs.: O tratamento com antireabsortivos, quando indicado, deve ser continuado pelo menos até que o tratamento de câncer de mama adjuvante seja finalizado ou por mais tempo nas mulheres com importante risco de fratura.
Tratamento preventivo da perda óssea acelerada pelo tratamento em pacientes com câncer de mama
Os estudos clínicos randomizados que avaliaram medidas para reduzir a perda óssea associada à terapia adjuvante do câncer de mama utilizaram medicamentos em doses e intervalos semelhantes ao tratamento da osteoporose pós-menopáusica.
As terapias anti-reabsortivas (bisfosfonatos), através da inibição dos osteoclastos, mostraram-se eficazes para estabilizar a DMO e reduzir a taxa de fraturas, atuando nas pacientes com câncer de mama no contexto adjuvante e no metastático. A eficácia destas terapias é influenciada pelo estado da menopausa e pela taxa de perda óssea.
O objetivo destas intervenções deve sempre visar à redução da taxa de fraturas por fragilidade como desfecho principal.
Exemplo de caso clínico
Paciente 71 anos, assintomática, com diagnóstico de câncer de mama receptor hormonal positivo. Realiza 1ª avaliação da massa óssea antes do tratamento adjuvante (figuras 2, 3 e 4):
Figura 2 – Densitometria óssea da coluna e do fêmur
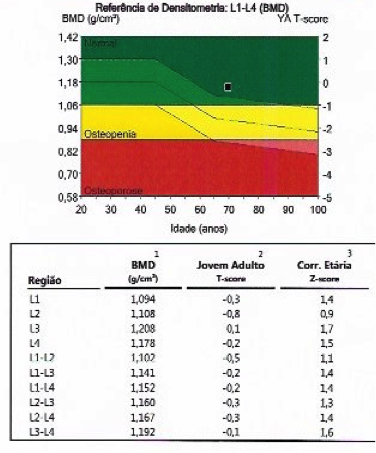
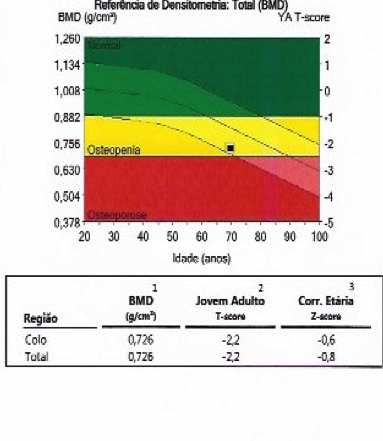
Resultado: Paciente apresenta osteopenia.
Figura 3 – Escore Trabecular – avaliação da microarquitetura trabecular
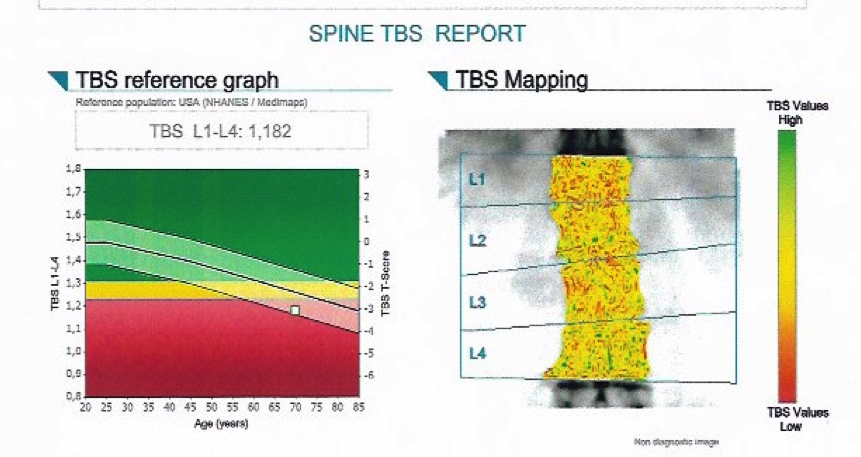
Resultado: escore trabecular compatível com microarquitetura degradada.
Figura 4 – Pesquisa de fratura por Densitometria- Vertebral Fracture Assessment (VFA)
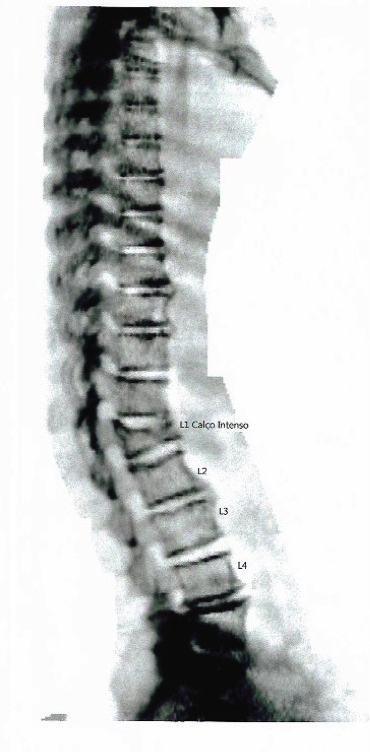
Resultado: fratura por fragilidade (osteoporose) em L1.
FRAX: Ferramenta para cálculo de risco de fratura em 10 anos
(https://www.sheffield.ac.uk/TBS/CalculationTool.aspx)
Idade: 71
Gênero: Feminino
Peso (kg): 56
Altura (cm): 153
IMC (kg/m²): 23.9
Fratura prévia: Sim
Pais com fratura de quadril: Não
Tabagismo atual: Não
Glicocorticóides: Não
Artrite reumatóide: Não
Osteoporose secundária: Não
Álcool 3 ou mais unidades/dia: Não
T-score de DMO do colo do fêmur: -2.2
TBS da coluna lombar: 1.182
Probabilidade de fratura nos próximos 10 anos (%) ajustada pelo TBS:
– Fratura maior por osteoporose: 11
– Fratura de quadril: 3,5 (acima do ponto de corte recomendável nos EUA: <3% em 10 anos)
Discussão: densitometria óssea: achados compatível com osteopenia, porém com escore trabecular baixo e compatível com microarquitetura trabecular degradada. Realizada a pesquisa de fratura por densitometria (Vertebral Fracture Assessment), mostrando fratura por fragilidade em L1 (osteoporose). Conclusão: paciente com osteoporose pela presença de fratura prévia por fragilidade, risco aumentado de fratura de quadril (3,5% em 10 anos). Conduta: orientações nutricionais, manutenção do peso adequado, mudança no estilo de vida, prevenção de quedas, início de tratamento antirreabsortivo durante o tratamento adjuvante e após o término, pelo alto risco de fratura.

Ana Lúcia Semmelmann
Médica Radiologista
Porto Alegre, RS
Referências:
- Adachi JD Corticosteroid-induced osteoporosis. Am J Med Sci. 1997 Jan;313(1):41-9
- Hadji P Cancer Treatment-Induced Bone Loss in women with breast câncer BoneKEy Reports 4, Article number: 692 (2015).
- Reid DM Guidance for the management of breast cancer treatment-induced bone loss: A consensus position statement from a UK Expert Group – Cancer Treat Rev. 2008;34 Suppl 1:S3-18.
- Coleman RE, Winter MC, Cameron D. The effects of adding zoledronic acid to neoadjuvant chemotherapy on tumour response: exploratory evidence for direct anti-tumour activity in breast cancer. Ir. J. Cancer. 2010; 102 : 1099-1105.
- Hadji P, Aapro MS, Body J-J, Gnant M, Brandi ML, Reginster JY, et al. Management of Aromatase Inhibitor-Associated Bone Loss (AIBL) in postmenopausal women with hormone sensitive breast cancer: Joint position statement of the IOF, CABS, ECTS, IEG, ESCEO, IMS, and SIOG. J Bone Oncol. 2017 Mar 23;7:1-12.
- Hadji P, Body JJ, Aapro MS Practical guidance for the management of aromatase inhibitor-associated bone loss. Ann. Oncol. 2008; 19 : 1407-1416.
- Kanis JA, McCloskey EV, Powles T, Paterson AH, Ashley S, Spector T. Uma alta incidência de fratura vertebral em mulheres com câncer de mama. Br J Cancer1999; 79 : 1179-1181.
- Rosa Maria Rodrigues Pereira, Jozélio Freire de Carvalho, Ana Patrícia Paula, Cristiano Zerbini et al. Diretrizes para a prevenção e tratamento da osteoporose induzida por glucorticoides Rev Braz Reumatol. 2012; 52 (4):569-593.

